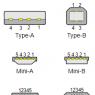
Cum măsoară testul virusului epstein barr. Virusul Epstein-Barr (infecție virală Epstein-Barr sau infecție EBV). Ce trebuie făcut dacă în timpul sarcinii sunt detectați anticorpi împotriva EBV
(EBV) este una dintre cele mai frecvente boli infecțioase umane. Anticorpii (Abs) la virusul Epstein-Barr (EBV) se gasesc la 60% dintre copii in primii doi ani de viata si la 80-100% dintre adulti. Incidența formei acute de EBVI (EBVI) în diferite regiuni ale lumii variază de la 40 la 80 de cazuri la 100 de mii de locuitori. Forma cronică a EBVI (CHEBVI) se dezvoltă la 15-25% dintre indivizi după EBVI. A fost stabilit rolul EBV în dezvoltarea neoplasmelor maligne, a bolilor autoimune și a sindromului de oboseală cronică. Toate acestea indică relevanța problemei EBVI.
EBV, descoperit în 1964 de M. Epstein și Y. Barr, aparține virusurilor γ-herpes. EBV are 3 antigene: capsid (VCA), precoce (EA) și nuclear (EBNA). Unicitatea procesului patologic în EBVI este determinată de capacitatea EBV de a transforma limfocitele B, persistența pe tot parcursul vieții în corpul uman, inducerea unei stări de imunodeficiență secundară (IDS), reacții autoimune și tumori maligne.
Sursa infecției cu EBV sunt pacienții cu forme manifeste și asimptomatice. 70-90% dintre persoanele care au avut EEBVI au eliminat virusul în următoarele 1-18 luni. Căi de transmitere a EBV: aerian, contact casnic, parenteral, sexual, vertical. OEBVI se caracterizează prin creșteri epidemice o dată la 6-7 ani, cel mai adesea înregistrate între 1 și 5 ani, în grupuri organizate.
Poarta de intrare pentru EBV este membrana mucoasă a tractului respirator superior: virusul pătrunde în țesutul limfoid, infectează limfocitele B, se dezvoltă activarea policlonală a limfocitelor B, diseminarea agentului patogen în limfocitele B, sinteza anticorpilor (Ab ) ca răspuns la stimularea antigenică este redusă. EBV afectează în primul rând organele limfoide (amigdale, ficat, splină).
Următoarea etapă este formarea unei clone de celule CD8 citotoxice sensibilizate, sinteza secvențială a Abs la antigenele VCA, EA și EBNA ale virusului. Din cauza unei încălcări a răspunsului imun, se formează activitatea funcțională a factorilor de rezistență înnăscuți (neutrofile, macrofage, celule NK, sistem interferon), IDS secundar.
Starea imunitară a 109 pacienți cu OEBVI cu vârsta cuprinsă între 5 și 14 ani în munca noastră a evidențiat semne de activare a componentei celulelor T a sistemului imunitar - o creștere a numărului de limfocite T (CD3), limfocite T citotoxice ( CD8), celule cu markeri de activare tardivă (HLA-DR); activarea policlonală a limfocitelor B - o creștere a numărului de celule CD20, imunoglobuline (Ig) IgA, IgM, IgG, complexe imune circulante (CIC). Au fost găsite semne de suprimare a sistemului imunitar: niveluri normale de celule T-helper (CD4), o scădere a indicelui imunoregulator CD4/CD8, numărul de celule NK natural killer (CD16) și o creștere a gradului de pregătire a imunocompetenților. celule pentru apoptoză (CD95). S-a observat activarea metabolismului dependent de oxigen al neutrofilelor și o reducere a capacităților sale de adaptare.
La o treime dintre copiii examinați (33,9%), EEBVI a apărut sub forma unei infecții mixte cu citomegalovirus (CMV), virusuri herpes simplex tipurile 1 și 2 (HSV-1, HSV-2). În timpul examinării bacteriologice a frotiurilor din orofaringe, 41,3% dintre pacienți au izolat Streptococcus (S.) viridans, 11,9% - Candida albicans, 8,2% - Staphylococcus (Staph.) epidermidis, 6,4% au S. piogenes, 2,7% - Klebsiella (Kl.) pneumoniae, 41,3% au avut o asociere de bacterii. 43,1% dintre pacienți au avut markeri serologici formă activă, 30,3% au avut micoplasmoză.
Următoarele rezultate ale CEBVI sunt posibile: infecție latentă, CEBVI, IDS, cancer, boli autoimune, . Trecerea la HEBVI este asociată cu un complex factori nefavorabiliîn perioadele ante, intra și postnatale, reglarea endocrină neuroimună afectată, predispoziție genetică.
Examinarea noastră a 60 de copii cu vârsta cuprinsă între 5 și 14 ani cu CEBVI a arătat că în acest grup 86,7% dintre mame aveau un istoric obstetrical complicat; La 83,3% dintre copii au fost depistate patologii perinatale și postnatale ale sistemului nervos central, organelor ORL etc.
Starea imunitară a pacienților cu CHEBVI a evidențiat o creștere a conținutului de antagonist al interleukinei-1 (IL-1RA), activarea insuficientă a celulelor imunocompetente (scăderea HLA-DR) și o creștere a gradului de pregătire pentru apoptoză (creșterea CD95). A existat o perturbare a activității funcționale a celulelor T helper de tip 1 (Th1) (niveluri scăzute de interferon y (IFN y)); scăderea numărului total de celule T (CD3), a numărului de limfocite cu receptori pentru IL-2 (CD25) și celule NK (CD16); conținutul de limfocite CD8 citotoxice a fost crescut. Persistența markerilor de replicare EBV pentru o lungă perioadă de timp în acest grup a indicat o încălcare a eliminării virusului; În același timp, o creștere a activității funcționale a Th2, activarea policlonală a limfocitelor B (CD20), o creștere a conținutului de IgA, IgM, IgG, CEC, o scădere a nivelului factorului chemotactic neutrofil (IL-). 8), și s-a observat o schimbare a metabolismului lor.
Tulburările stării imune au dus la activarea microflorei oportuniste, a infecțiilor virale și fungice. În spectrul microbian al mucoasei orofaringiene la pacienții cu CHEBVI, S. viridans (30%), Candida albicans (28,3%), Stafilococ. Epidermidis (25%), S. pyogenes (20%), Kl. Pneumoniae(8,4%), asociere bacteriană (41,7%); 28,3% au avut markeri serologici ai formei active de chlamydia, 26,7% au avut micoplasmoză. La 90% dintre pacienți, boala a apărut sub forma unei infecții mixte care implică: EBV + CMV, EBV + HSV-1, HSV-2.
Clasificare. Nu există o clasificare general acceptată a bolii; Vă recomandăm să utilizați clasificarea de lucru a EBVI pe care am dezvoltat-o.
- După perioada de apariție: congenital, dobândit.
- Sub formă: tipic (mononucleoză infecțioasă), atipic: șters, asimptomatic, visceral.
- După gravitate: ușor, mediu, greu.
- Conform cursului: acut, prelungit, cronic.
- După fază: activ, inactiv.
- Complicatii: hepatita, ruptura splenica, meningoencefalita, poliradiculoneuropatie, miocardita, sinuzita, otita, anemie hemolitica, trombocitopenie, neutropenie, pancreatita etc.
- Infecție mixtă.
Exemple de diagnostic:
- De bază: EBVI dobândit, formă severă tipică (), curs acut, fază activă. Măgar:
- De bază: EBVI dobândit, formă viscerală (meningoencefalită, hepatită, nefrită), curs cronic sever, fază activă. Măgar: insuficienta hepatico-renala acuta. Comp.: Chlamydia respiratorie (,).
Tabloul clinic al EBVI acut a fost descris pentru prima dată de N.F Filatov (1885) și E. Pfeiffer (1889). Perioada de incubație durează de la 4 zile la 7 săptămâni. Un complex complet de simptome se formează în a 4-10-a zi de boală.
Am examinat 109 copii cu OEBVI. La majoritatea pacienților, boala debutează acut, cu creșterea temperaturii corpului și apariția simptomelor de intoxicație; mai rar, se observă un debut gradual: timp de câteva zile există stare de rău, slăbiciune, letargie și pierderea poftei de mâncare. Temperatura corpului este subfebrilă sau normală. În a 2-a-4-a zile de boală, temperatura ajunge la 39-40 ° C; febra si simptomele de intoxicatie pot persista 2-3 saptamani sau mai mult.
Limfadenopatia generalizată este un simptom patognomonic al EBVI și din primele zile ale bolii se manifestă sub formă de afectare sistemică a 5-6 grupe de ganglioni limfatici (LN), cu o creștere predominantă de până la 1-3 cm în diametrul LN-urile cervicale anterioare și posterioare, submandibulare. LN-urile sunt ușor dureroase la palpare, nu sunt fuzionate între ele și cu țesuturile din jur și sunt aranjate sub forma unui „lanț” sau „pachet”; vizibil la întoarcerea capului, dându-i gâtului un contur „încărcat”. Uneori există o pastilitate a țesuturilor moi peste ganglionii limfatici măriți.
- cel mai frecvent și precoce simptom al OEBVI, însoțit de mărirea amigdalelor la gradul II-III. Modelul lacunar este accentuat din cauza infiltrării țesutului amigdalelor sau netezit din cauza limfostazei. Pe amigdale există plăci de culoare alb-gălbui sau gri murdar sub formă de insule și dungi. Acestea provin din goluri, au o suprafață aspră (amintește de dantelă), se îndepărtează ușor fără sângerare, se frecă și nu se scufundă în apă. Există o discrepanță între dimensiunea plăcii și gradul de mărire a ganglionilor limfatici regionali. Cu caracterul fibrinos-necrotic al plăcilor, dacă se răspândesc dincolo de amigdale, este necesar un diagnostic diferențial cu difterie. Plăcile de pe amigdale dispar de obicei după 5-10 zile.
Semnele de adenoidite se găsesc la marea majoritate a pacienților. Există congestie nazală, dificultăți în respirația nazală, sforăit cu gura deschisă, mai ales în timpul somnului. Fața pacientului capătă un aspect „adenoid”: umflături, pastecire a pleoapelor, puntea nasului, respirație pe gură deschisă, buze uscate.
Hepatomegalia poate fi detectată încă din primele zile ale bolii, dar este depistată mai des în a doua săptămână. Normalizarea dimensiunii ficatului are loc în decurs de șase luni. La 15-20% dintre pacienți, hepatita se dezvoltă ca o complicație.
Splenomegalia este un simptom tardiv și apare la majoritatea pacienților. Normalizarea dimensiunii splinei are loc în 1-3 săptămâni.
Exantemul cu OEBVI apare in zilele 3-14 ale bolii, are caracter polimorf - patat, papular, maculopapular, rozolos, punctat, hemoragic. Nu există o localizare specifică. Erupția durează 4-10 zile, uneori lăsând pigmentarea. La copiii tratați cu ampicilină sau amoxicilină, erupția apare mai des (90-100%).
Modificările hematologice includ leucocitoza (10-30 x 10 9 /l), neutropenie cu o deplasare a benzii spre stânga, creșterea numărului de limfocite, monocite, celule mononucleare atipice până la 50-80%, creșterea VSH până la 20-30 mm/oră. Un semn hematologic caracteristic sunt celulele mononucleare atipice în cantitate de 10-50%: apar până la sfârșitul primei săptămâni de boală și persistă 1-3 săptămâni.
EBVI cronică este rezultatul OEBVI sau se dezvoltă ca formă cronică primară. Am examinat 60 de copii cu CHEBVI, al căror tablou clinic a inclus sindromul asemănător mononucleozei cronice și patologia multiplă de organe. S-a constatat că toți pacienții prezintă sindrom limfoproliferativ (limfadenopatie generalizată, hipertrofie a amigdalelor palatine și faringiene, mărirea ficatului și splinei) și semne de intoxicație cronică (febră prelungită de grad scăzut, slăbiciune, pierderea poftei de mâncare etc.). Datorită dezvoltării IDS, au fost observate organe acute și ORL cu exacerbări de până la 6-11 ori pe an: rinofaringită (28,3%), faringoamigdalite (91,7%), adenoidită (56,7%), otită (11,7%), sinuzită ( 20%), laringotraheită (18,3%), bronșită (38,3%), pneumonie (25%). De remarcat a fost frecvența ridicată a patologiei de organe multiple cauzată de replicarea pe termen lung a EBV, IDS secundar și reacții autoimune (patologie SNC; sindrom cardiac, artralgie).
ÎN ultimii ani a fost descrisă EBVI congenital. S-a stabilit că riscul său cu EBVI primar în timpul sarcinii este de 67%, cu reactivare - 22%. Tabloul clinic al EBVI congenital este similar cu cel al CMVI.
Rolul EBV în dezvoltarea cancerului și a proceselor paraneoplazice a fost stabilit - limfomul Burkett, carcinomul nazofaringian, limfogranulomatoza, tumorile stomacului, intestinelor, glandelor salivare, uterului, leucoplaziei limbii și mucoasei bucale, precum și o serie de boli autoimune - pneumonită interstițială limfoidă, uveită etc. EBV, împreună cu virusurile herpetice umane tipurile 6 și 7, este un factor etiologic și cel mai mult cauza comuna(15%) dezvoltarea febrei prelungite de origine necunoscută.
Diagnosticul EBVI pe baza luării în considerare a grupurilor de risc, a sindroamelor clinice de conducere și a datelor cercetare de laborator. Grupurile de risc ale mamei includ un istoric medical împovărat, markeri ai infecțiilor virale cu herpes etc., la copil - leziuni perinatale ale sistemului nervos central, fenotip alergic, IDS, markeri ai infecțiilor virale herpes etc. Principalele sindroame clinice ale EBVI sunt sindroame asemănătoare mononucleozei, sindroame infecțioase generale, exantem, sindrom de patologie multiplă de organe.
Standardul obligatoriu pentru diagnosticarea EBVI include un test clinic de sânge, o analiză generală a urinei, un test biochimic de sânge, un examen bacteriologic al mucusului orofaringelui și al nasului, markeri serologici ai EBV, alți virusuri herpetice, chlamydia, micoplasme, ecografie abdominală. organe, consultarea medicului ORL, dacă este indicat - radiografia sinusurilor și organelor paranazale piept, ECG. Standard de diagnostic suplimentar (într-o instituție specializată de tratament și profilactic): markeri ai EBV, altor virusuri herpetice, chlamydia, micoplasme folosind reacția în lanț a polimerazei (PCR), imunogramă de nivel doi, consultarea unui imunolog, dacă este indicat - coagulogramă, tablou morfologic al puncție sternală, consultație cu un hematolog, oncolog.
Metoda imunoenzimatică (ELISA) este utilizată pentru a determina Abs la antigenele EBV, ceea ce permite diagnosticul de laborator al EBV și determinarea perioadei procesului infecțios.
Anticorpii din clasa IgM la VCA apar concomitent cu manifestările clinice ale EBV, persistă timp de 2-3 luni și sunt resintetizați în timpul reactivării EBV. Persistența pe termen lung a titrurilor mari ale acestor Abs este caracteristică CHEBVI, tumorilor induse de EBV, bolilor autoimune și IDS.
Anticorpii din clasa IgG împotriva EA ating un titru ridicat în a 3-4-a săptămână de OEBVI și dispar după 2-6 luni. Ele apar în timpul reactivării și sunt absente în forma atipică de EBVI. Titruri mari de Abs din această clasă sunt detectate în cazurile de CHEBVI, boli oncologice și autoimune induse de EBV și IDS.
Anticorpii IgG la EBNA apar la 1-6 luni după infecția primară. Apoi titrul lor scade și persistă pe tot parcursul vieții. Când EBVI este reactivat, titrul lor crește din nou.
Studiul avidității IgG clasa Ab (puterea legării antigenului la Ab) este de mare importanță. În timpul infecției primare, Abs cu aviditate scăzută (indicele de aviditate (AI) mai mic de 30%) sunt mai întâi sintetizați. Stadiul târziu al infecției primare se caracterizează prin Abs cu aviditate medie (IA - 30-49%). Abs cu aviditate ridicată (IA - mai mult de 50%) se formează la 1-7 luni după infectarea cu EBV.
Markerii serologici ai fazei active a EBVI sunt IgM Abs la VCA și IgG Abs la EA, IgG Abs cu aviditate scăzută și medie la markerii fazei inactive, IgG Abs la EBNA.
Materialele pentru PCR sunt sânge, lichid cefalorahidian, saliva, frotiuri din mucoasa orofaringiană, biopsii de organe etc. Sensibilitatea PCR pentru EBVI (70-75%) este mai mică decât pentru alte infecții cu herpesvirus (95-100%). Acest lucru se datorează apariției EBV în fluidele biologice numai în timpul lizei mediate imun a limfocitelor B infectate.
Tratament. Principiile tratamentului pentru EBVI sunt complexe, utilizarea medicamentelor etiotrope, continuitatea, durata și continuitatea măsurilor de tratament la etapele „spital → clinică → centru de reabilitare”, monitorizarea parametrilor clinici și de laborator.
Pe baza experienței de a trata 169 de copii cu EBVI, am dezvoltat un standard de tratament pentru această boală.
Terapie de bază: regim de protectie; nutriție terapeutică; medicamente antivirale: medicamente virocide - inozin pranobex (Isoprinosine), nucleozide anormale (Valtrex, Acyclovir), Arbidol; Preparate de IFN - IFN recombinant α-2β (Viferon), Kipferon, Reaferon-ES-Lipint, interferoni pentru administrare intramusculară (Reaferon-EC, Realdiron, Intron A, Roferon A etc.); Inductori IFN - Amiksin, doze ultra-scăzute de anticorpi la γ-IFN (Anaferon), Cycloferon, Neovir. După indicații: medicamente antibacteriene locale (Bioparox, Lizobakt, Stopangin etc.); medicamente antibacteriene sistemice (cefalosporine, macrolide, carbapeneme); imunoglobuline pentru administrare intravenoasă (Imunovenin, Gabriglobin, Intraglobin, Pentaglobin etc.); complexe de vitamine și minerale - Multi-tabs, Vibovit, Sanasol, Kinder Biovital gel etc.
Intensificarea terapiei de bază conform indicațiilor:
Terapie imunocorectivă sub controlul unei imunograme - imunomodulatoare (Polyoxidonium, Likopid, Ribomunil, IRS-19, Imudon, Derinat etc.), citokine (Roncoleukin, Leukinferon); probiotice (Bifiform, Acipol etc.); medicamente de reabilitare metabolică (Actovegin, Solcoseryl, Elkar etc.); enterosorbenti (Smecta, Filtrum, Enterosgel, Polyphepan etc.); antihistaminice de a doua generație (Claritin, Zyrtec, Fenistil etc.); hepatoprotectori (Hofitol, Galstena etc.); glucocorticosteroizi (prednisolon, dexametazonă); inhibitori de protează (Kontrikal, Gordox); neuro- și angioprotectori (Encephabol, Gliatilin, Instenon etc.); medicamente „cardiotrope” (riboxină, cocarboxilază, citocrom C etc.); remedii homeopate și antihomotoxice (Ocillococcinum, Aflubin, Lymphomyosot, Tonzilla compositum etc.); metode non-medicamentale (terapie cu laser, terapie magnetică, acupunctură, masaj, kinetoterapie etc.)
Terapie simptomatică.
Pentru febră - medicamente antipiretice (paracetamol, ibuprofen etc.); dacă există dificultăți în respirația nazală - medicamente nazale (Isofra, Polydexa, Nazivin, Vibrocil, Adrianol etc.); pentru tuse uscată - medicamente antitusive (Glauvent, Libexin), pentru tuse umedă - expectorante și medicamente mucolitice (AmbroHEXAL, bromhexină, acetilcisteină etc.).
Timp de câțiva ani, pentru tratamentul EBVI, am folosit cu succes un regim de terapie etiotropă combinată treptat, care include inozin pranobex (Isoprinozină) și interferon recombinant α-2β (Viferon) (Fig. 1, 2). Inosine pranobex (Isoprinosine) suprimă sinteza proteinelor virale și inhibă replicarea unei game largi de virusuri ADN și ARN, inclusiv EBV. Medicamentul are activitate imunocorectivă - modulează răspunsul imun în funcție de tipul celular, stimulează producția de Abs, citokine, IFN, crește activitatea funcțională a macrofagelor, neutrofilelor și celulelor NK; protejează celulele afectate de scăderea post-virală a sintezei proteinelor. Inozin pranobex (Isoprinosine) a fost prescris in doza de 50-100 mg/kg/zi pe cale orala in 3-4 prize. Au fost efectuate trei cure de tratament timp de 10 zile cu un interval de 10 zile. IFN recombinant α-2β (Viferon) inhibă replicarea virală prin activarea endonucleazei și distrugerea ARN-ului mesager viral. Medicamentul modulează răspunsul imun, promovează diferențierea limfocitelor B, stimulează producția de citokine și crește activitatea funcțională a macrofagelor, neutrofilelor și celulelor NK. Antioxidanții naturali pe care îi conține (vitaminele E și C) stabilizează membranele celulare. Medicamentul a fost prescris conform unui regim prelungit (V.V. Malinovskoy et al., 2006).
Eficacitatea terapiei etiotrope pentru OEBVI a fost evaluată în două grupuri de pacienți. Pacienții din primul grup (52 de persoane) au primit inozin pranobex (Isoprinozină) în combinație cu IFN α-2β recombinant (Viferon), pacienții din grupul 2 (57 de copii) au primit monoterapie cu IFN α-2β recombinant (Viferon). Parametrii clinici și serologici înainte de începerea tratamentului și după 3 luni de terapie sunt prezentați în . La pacienții din ambele grupuri, de-a lungul timpului s-a observat o scădere semnificativă a simptomelor precum limfadenopatia generalizată, amigdalita, adenoidita, hepatomegalia și splenomegalia. Cu toate acestea, pe fondul terapiei combinate, dinamica pozitivă a indicatorilor clinici a fost mai semnificativă; infecții respiratorii acute (IRA) doar la 19,2% dintre pacienții din grupul 1 și la 40,3% dintre pacienții din grupul 2 (p< 0,05). На фоне комбинированной терапии наблюдалось более быстрое исчезновение серологических маркеров репликации.
Terapia combinată pentru OEBVI a contribuit la modularea răspunsului imun în funcție de tipul de celule (creșterea limfocitelor CD3-, CD4-, CD8-, CD16- și HLA-DRT). Pregătirea celulelor imunocompetente pentru apoptoză (CD95) a scăzut. A existat stimularea producției de IgA, schimbarea sintezei Ab de la IgM la IgG, o scădere a conținutului de CEC și rate metabolice îmbunătățite ale neutrofilelor.
Eficacitatea terapiei etiotrope a fost studiată la 60 de pacienți cu CHEBVI. Pacienții din grupul 1 (30 de copii) au primit inozin pranobex (Isoprinozină) și IFN α-2β recombinant (Viferon), grupul 2 (30 de persoane) au primit monoterapie cu IFN α-2β recombinant (Viferon). Indiferent de regimul de tratament, la 3 luni de la începerea terapiei, s-a observat o scădere semnificativă a frecvenței limfadenopatiilor generalizate, hipertrofia amigdalelor palatine și faringiene, splenomegalie, intoxicație, sindroame infecțioase și vegetativ-viscerale ( ). Combinația de inozin pranobex (Isoprinozină) cu IFN α-2β recombinant (Viferon) a contribuit la o dinamică mai semnificativă a parametrilor clinici. Numărul de episoade IRA a scăzut de la 6-11 (7,9 ± 1,1) la 4-6 (5,2 ± 1,2) pe an în timpul monoterapiei cu IFN α-2β recombinant (Viferon) și la 2-4 (2,5 ± 1,4) pe an în timpul terapiei combinate (pag< 0,05). В обеих группах уменьшалась частота репликации ВЭБ, однако при сочетанном применении противовирусных препаратов этот эффект был более выраженным.
Utilizarea unei combinații de inozin pranobex (Isoprinozină) și IFN α-2β recombinant (Viferon) la pacienții cu CEBVI a condus la o dinamică pozitivă mai pronunțată a indicatorilor stării imune (scăderea conținutului de IL-1RA, normalizarea expresiei markerilor de activare ai celule imunocompetente (HLA-DR) și receptori de apoptoză (CD95 creșterea activității funcționale a Th1 (creșterea IFN γ), restabilirea numărului de limfocite T și celule NK, mai mare decât în monoterapie, conținutul de limfocite CD8 nu sa normalizat complet; expresia receptorului IL-2 (CD25) în timpul terapiei antivirale combinate, activitatea funcțională a Th2 a scăzut (nivelul de IL-4 sa normalizat) nu a atins norma. dar a fost mai mare decât la monoterapie cu Viferon.
Nu au existat efecte secundare la utilizarea inozină pranobex (Isoprinozină) și IFN α-2β recombinant (Viferon).
Rezultatele studiului indică potențarea efectelor combinației de inozin pranobex (Isoprinozină) cu IFN a-2b recombinant (Viferon) la pacienții cu EBVI.
Potențarea efectelor antivirale, imunomodulatoare și citoprotectoare ale acestor medicamente duce la o dinamică pozitivă mai semnificativă a manifestărilor simptomelor clinice ale EBVI decât cu monoterapie și la dispariția markerilor serologici ai activității procesului infecțios. Trebuie remarcat eficiența ridicată și siguranța terapiei combinate folosind inozin pranobex (Isoprinozină) și IFN α-2β recombinant (Viferon).
Reabilitare. Copilul este observat de un medic local și de un specialist în boli infecțioase și este scos din registru la 6-12 luni de la dispariția indicatorilor clinici și de laborator ai activității procesului infecțios. Frecvența inspecțiilor este de 1 dată pe lună. Conform indicațiilor, se recomandă consultarea unui medic ORL, imunolog, hematolog, oncolog etc. Studiile de laborator și instrumentale ale pacienților includ: analiză clinică de sânge o dată pe lună timp de 3 luni, apoi o dată la 3 luni, mai des dacă este indicat. ; markeri serologici ai EBV folosind ELISA o dată la trei luni, mai des dacă este indicat; PCR de sânge, frotiuri orofaringiene o dată la 3 luni, mai des dacă este indicat; imunograma - o dată la 3-6 luni; studii biochimice şi instrumentale – conform indicaţiilor.
Terapia de reabilitare include: regimul protector, terapia nutrițională, medicamentele antivirale după regimuri prelungite. Sub controlul imunogramei se efectuează imunocorecția. Conform indicațiilor, medicamente antibacteriene locale, cursuri de complexe vitamino-minerale, pro- și prebiotice, medicamente de reabilitare metabolică, enterosorbanți, antihistaminice, hepato-, neuro- și angioprotectori, medicamente cardiotrope, enzime, remedii homeopate și metode de tratament non-medicament sunt prescrise.
Astfel, EBVI se caracterizează printr-o distribuție largă, un curs lung cu reactivare periodică a procesului infecțios la unii pacienți, posibilitatea dezvoltării complicațiilor și a rezultatelor adverse (boli oncologice, patologie autoimună). Formarea IDS secundar joacă un rol important în EBVI. Principalele sindroame clinice ale EBVI sunt sindroamele asemănătoare mononucleozei acute și cronice, intoxicația, sindroamele infecțioase, cerebrale, gastrointestinale, cardiace și artralgice. Diagnosticul EBVI se bazează pe analiza grupurilor de risc, identificarea sindroamelor clinice de top și testele de laborator. Tratamentul EBVI este complex și include medicamente etiotrope (medicamente virostatice, interferon și inductorii săi), medicamente pentru terapie patogenetică, imunomodulatoare și simptomatică. Utilizarea combinată prelungită a inozin-pranobex (Isoprinozină) și IFN α-2β recombinant (Viferon), potențizând efectele lor imunocorectoare și citoprotectoare, crește semnificativ eficacitatea tratamentului. Pacienții cu EBVI au nevoie de reabilitare pe termen lung cu monitorizarea obligatorie a indicatorilor clinici și de laborator ai activității procesului infecțios.
Pentru întrebări referitoare la literatură, vă rugăm să contactați editorul.
E. N. Simovanyan, Doctor în Științe Medicale, Profesor
V. B. Denisenko, Candidat la Științe Medicale
L. F. Bovtalo, Candidat la Științe Medicale
A. V. Grigorian
Universitatea de Stat de Medicină Rostov, Rostov-pe-Don
Infecția cu virusul Epstein-Barr apare în copilărie sau adolescență și poate exista în stare ascunsă aproape toată viața mea. Diagnosticul virusului Epstein Barr se bazează pe tabloul clinic și pe teste de laborator, în care se determină markerii serologici sau se confirmă prezența infecției în diferite fluide biologice prin metoda PCR. Prezența celulelor specifice (celule mononucleare) sau a anticorpilor în sânge este principalul criteriu de diagnostic în absența simptomelor clare.
Indicații pentru diagnostic
Motivele efectuării analizelor care determină (VEB) sunt următoarele:
- imunitate slabă;
- ganglioni limfatici măriți (submandibulari, occipitali);
- leucopenie;
- simptome caracteristice ale mononucleozei infecțioase.
Diagnosticul diferențial al mononucleozei infecțioase se realizează cu leucemie acută, gripă sau ARVI, care apar cu crestere semnificativa ganglionii limfatici regionali, precum și rujeola și rubeola. Mononucleoza poate fi combinată cu. Pentru a clarifica, ar trebui să faceți un test pentru anticorpi împotriva citomegalovirusului.
Tipuri de teste de laborator
Testele de laborator sunt efectuate folosind metodele ELISA (enzyme-linked immunosorbent assay) și PCR (reacția în lanț a polimerazei). Testul heterofil este efectuat ca un studiu suplimentar în diagnosticul mononucleozei infecțioase cauzate de virusul Epstein-Barr. Un test de sânge biochimic indică indirect modificări hematogene.
Test clinic de sânge pentru virusul Epstein-Barr
 Abaterile de la normă necesită diagnosticare suplimentară de laborator.
Abaterile de la normă necesită diagnosticare suplimentară de laborator. Dacă se suspectează EBV, un test general de sânge cu număr de leucocite este foarte informativ. În perioada acută a bolii, într-o probă de sânge capilar al pacientului, un tehnician de laborator calificat detectează apariția celulelor mononucleare, detectează un conținut crescut de limfocite, trombocite, observă o scădere a concentrației de eritrocite și o scădere a hemoglobinei. . Pentru a confirma sau infirma diagnosticul de mononucleoză infecțioasă, sunt necesare examinări suplimentare.
Biochimia sângelui
Rezultatele analizei biochimice oferă informații despre reacțiile metabolice din organism. Nu există indicatori specifici în studiul biochimic care să fie caracteristici invaziei EBV. Valorile transaminazelor, enzimelor, proteinelor (fibrinogen, CRP) vor fi crescute. Dar aceste modificări nu vor confirma prezența virusului Epstein-Barr.
Cercetare PCR
PCR este o metodă de cercetare de laborator care are ca scop detectarea agentului cauzal al unei boli infecțioase. Analiza detectează virusul Epstein-Barr la concentrațiile sale minime din organism. Metoda se bazează pe detectarea ADN-ului viral. Atunci când se efectuează cercetări, sunt necesare mostre de biomateriale:
- sânge;
- urină;
- salivă;
- spută.
 Studiul este efectuat în timpul exacerbării bolii.
Studiul este efectuat în timpul exacerbării bolii. În laboratoare, sângele este de obicei luat dintr-o venă pentru testare. Rezultatele testelor sunt evaluate calitativ - dacă virusul este absent sau prezent în organism. Dezavantajul studiului este că este eficient în perioada acută. Dacă boala s-a manifestat mai devreme, reacția polimerică în lanț nu este prescrisă. Studiul este relevant dacă este necesar să se determine prezența virusului Epstein-Barr la nou-născuți. Reacțiile serologice din această perioadă sunt ineficiente din cauza imaturității sistemului imunitar al sugarilor.
Testul heterofil
Studiul este efectuat pentru a detecta heterofile anticorpi EBVîn plasma sanguină fără fibrinogen. Acest test este metoda suplimentara la diagnosticul EBV. Producerea de anticorpi specifici eterogene este un răspuns la infecția cu virusul Epstein-Barr. Acestea includ:
- factor reumatic;
- anticorpi antinucleari;
- aglutinine reci.
Toți indicatorii de mai sus se referă la aglutininele din clasa IgM. Sunt produse în primele 7-14 zile de la momentul infectarii. Nivelul lor crește treptat și atinge un număr maxim până la sfârșitul primei luni de boală. Apoi cantitatea de anticorpi scade ușor. Aglutininele din clasa IgM se găsesc în fluxul sanguin în perioada de convalescență.
(VEB, EBV) aparține familiei virusului herpes 4, are antigeni care îi determină proprietățile infecțioase. Un test de sânge pentru prezența virusurilor Epstein-Barr în corpul uman constă în detectarea anticorpilor (AT) la antigenele virale (AG) folosind metode serologice.
Mononucleoza infecțioasă este contractată în copilărie, iar 9 din 10 adulți au dezvoltat imunitate stabilă la această boală. Dar, ca și alți virusuri herpetice, infecția cu EBV poate exista în organism pentru o lungă perioadă de timp, iar persoana însuși este purtătoare de virus.
Prezența infecției în corpul uman este confirmată sau infirmată folosind:
- teste serologice;
- diagnostic molecular - metoda PCR.
Aceste teste precise fac posibilă nu numai evaluarea modificărilor apărute în formula de sânge, ci și determinarea cu exactitate a cantității și a tipurilor de anticorpi care s-au format pentru a lupta împotriva infecțiilor în organism.
Prin efectuarea și interpretarea unui test de ser sanguin pentru anticorpi împotriva Ag al virusului Epstein-Barr, sunt identificate formele active, cronice și latente ale bolii mononucleozei infecțioase.
Metode de diagnosticare
Principalele metode de diagnosticare a mononucleozei infecțioase includ detectarea prezenței anticorpilor la antigenele virale. Cercetările se efectuează cu ajutorul testelor serologice. Serologia este știința proprietăților serului sanguin.
Procesele care au loc în serul sanguin sunt studiate de imunologie, iar principalele interacțiuni au loc între moleculele proteice - proteinele AT proprii ale corpului, care sunt produse de limfocitele B, și proteinele antigen străine. În cazul mononucleozei infecțioase, proteinele virale acționează ca antigene.
O metodă suplimentară de confirmare a infecției cu EBV este o metodă numită reacție în lanț a polimerazei (PCR), care va fi discutată mai jos.
La diagnosticare, sunt utilizate și date din studiile privind prezența anticorpilor IgA la antigenele virusului. Această metodă este utilizată pentru a diagnostica cancerul nazofaringian.
Rezultatele testelor pot fi:
- pozitiv, ceea ce înseamnă stadiul bolii în formă acută, cronică, latentă sau procesul de recuperare;
- negativ, ceea ce poate însemna absența infecției, stadiul inițial (prodromal), o formă inactivă de infecție;
- îndoielnic - în acest caz, analiza se repetă după 2 săptămâni.
Anticorpi heterofili
Apariția infecției virale Epstein Barr în sânge declanșează proliferarea limfocitelor B și producerea număr mare Imunoglobuline IgM, neobișnuite prin structura și compoziția lor.
Astfel de IgM aleatoare, neobișnuite, pe care limfocitele B infectate cu virus le produc în mod activ în sânge, se numesc Abs Paul-Bunnel heterofile. Proteinele heterofile sunt detectate prin metoda de aglutinare cu eritrocite de oi, cai și tauri după un tratament special.
IgM heterofilă este detectată în sânge până la 6 luni de la data infecției. Acest test este considerat specific adulților. Fiabilitatea sa în această categorie de vârstă este de 98-99%.
Dar la copii, mai ales sub vârsta de 2 ani, specificitatea testelor pentru prezența virusurilor Epstein Barr în organism este de doar 30%. Odată cu vârsta, specificitatea analizei crește, dar și în acest caz, testul pentru IgM heterofil poate fi pozitiv la copii și cu alte infecții virale.
Modificări similare ale serului sanguin, însoțite de apariția IgM heterofile, apar în sânge în timpul infecției cu citomegalovirus, infecțiilor respiratorii acute, varicelei, rujeolei și toxoplasmozei.
Rezultatele testului pentru anticorpi IgM heterofili pot fi:
- fals negativ – la copiii sub 4 ani, precum și în primele 2 săptămâni de la debutul mononucleozei infecțioase;
- fals pozitiv – pentru oreion, pancreatită, hepatită, limfoame.
Studii serologice
Mai mult mod exact Diagnosticul infecției cu mononucleoză infecțioasă se realizează prin detectarea anticorpilor împotriva virusurilor Epstein Barr. Studiile serologice sunt efectuate prin izolarea anticorpilor din serul sanguin, care aparțin imunoglobulinelor IgM și imunoglobulinelor IgG.
Anticorpii se formează ca răspuns la prezența antigenelor virusului Epstein-Barr în serul sanguin:
- antigen timpuriu - EA (antigen timpuriu), conține componente care sunt desemnate D și R;
- antigen de membrană – MA (antigen de membrană);
- antigen nuclear (nuclear) – EBNA (antigen nucleic Epstein-Barr);
- antigen capside – VCA (antigen capsid virus).
La aproape toți pacienții aflați în faza acută a bolii, se observă prezența anticorpilor IgG la antigenul capsidei. Anticorpii IgG se disting prin faptul că persistă toată viața.
Anticorpii IgM sunt detectați la toți pacienții cu mononucleoză infecțioasă în medie la 14 zile după infecție, dar adesea dispar fără urmă după 2-3 luni.
Metodele de detectare a anticorpilor împotriva EBV sunt:
- NIF - metoda fluorescenței indirecte - sunt detectați anticorpi IgG, IgM împotriva virusului Epstein-Barr produși la EA și VCA;
- fluorescență anti-complement - găsește anticorpi care sunt produși pentru Infecții cu EBV ca răspuns la prezența antigenelor EBNA, EA, VCA;
- ELISA – test imunosorbent legat de enzime.
Antigen precoce
Antigenul EA timpuriu, care apare pentru prima dată după infecție, este numit și difuz, deoarece se găsește atât în nucleele, cât și în citoplasma limfocitelor B infectate. Antigenele care se găsesc numai în citoplasma limfocitelor B se numesc citoplasmatice.
Anticorpii împotriva EA sunt produși în stadiile inițiale ale infecției. Anticorpii la componenta D pot apărea în stadiu perioadă incubațieși să nu fie descoperite niciodată ulterior.
AT la componenta R EA începe să apară la 21 de zile după apariția simptomelor de infecție și persistă în organism timp de un an. Acești anticorpi sunt detectați în limfomul Burkitt, boli autoimune provocate de EBV și imunodeficiență.
După ce pacientul își revine din mononucleoza infecțioasă, infecția virală EBV persistă în limfocitele B. Acest lucru creează un risc de reactivare a virușilor Epstein-Barr. În acest caz, se efectuează o analiză pentru prezența anticorpilor pentru difuzarea hipertensiunii precoce.
Antigenul capsidei
O caracteristică importantă care confirmă infecția cu virusul Epstein-Barr este detectarea anticorpilor IgG la antigenul capsidei.
Anticorpii la antigenele capsidei virusurilor Epstein-Barr (EBV) se gasesc sub forma a 2 clase principale de imunoglobuline - anti - VCA IgGși IgM.
Anticorpii împotriva proteinei capsidelor persistă pe tot parcursul vieții. Uneori pot fi găsite pe stadii incipiente, dar mai des cea mai mare concentrație de anticorpi la antigenul capsidei VCA IgG, precum și hipertensiunea precoce, se observă la 8 săptămâni de la momentul infectării cu virusurile Epstein Barr.
Un test pozitiv, care se obține la testarea pentru IgG AT (anticorpi) la proteinele capsidei virusului Epstein Barr, înseamnă că s-a format imunitatea în organism și acest lucru face ca persoana să fie rezistentă la infecția cu VEB în viitor.
- Un test pozitiv pentru detectarea anticorpilor IgG la antigenul capsidei la titruri mari în timpul infecției cu virusul Epstein Barr indică o infecție cronică.
- Un test negativ pentru proteinele capside IgG nu exclude faza acută a bolii dacă testul a fost efectuat imediat după infectare.
Înainte ca simptomele infecției să apară în sânge, apar anticorpi IgM la antigenul capsidei. Descifrarea faptului prezenței anticorpilor IgM în serul sanguin în testele pentru virusurile Epstein Barr poate fi chiar începutul mononucleozei infecțioase sau al fazei sale acute.
O concentrație mare de anticorpi IgM în sânge la proteina antigenică a capsidei este detectată în primele 6 săptămâni după infecție. Titrurile scăzute de anticorpi pot indica o infecție recentă.
Antigenul nuclear
Anticorpii împotriva antigenului nuclear viral apar târziu în cursul infecției. Un test pozitiv pentru prezența anticorpilor IgG împotriva antigenului nuclear (antigen nuclear) EBNA al virusului Epstein Barr indică stadiul de recuperare.
Căutarea prezenței anticorpilor IgG, care sunt produși împotriva antigenului NA (proteina antigenică nucleară) al virusului Epstein Barr, poate da un rezultat pozitiv pentru mulți ani după boală.
Un test pozitiv pentru anticorpi IgG la antigenul nuclear, dar un rezultat negativ pentru prezența anticorpilor IgM la antigenul capside al virusului Epstein-Barr, înseamnă că există un focar de inflamație infecțioasă în organism.
Teste serologice în serul sanguin pentru prezența anticorpilor împotriva virusului Epstein-Barr. Abreviere: IM – mononucleoză infecțioasă, CN – carcinom nazofaringian, LB – limfom Burkitt.
| Starea pacientului | AT heterofil | Antigenul IgG anti-capside | Anticorpi IgM la antigenul capsidei | AT pentru a difuza hipertensiunea arterială | AT împotriva hipertensiunii precoce | AT la nuclear AG |
| EI | * | * | ** | * | — | — |
| Recuperare după MI | * | — | * | — | * | * |
| MI anterior | — | — | * | — | — | * |
| Reactivarea MI | — | — | ** | * | * | * |
| KN | — | — | *** | ** | * | * |
| LIVRE | — | — | *** | ** | * | * |
PCR
Cea mai informativă modalitate de a diagnostica infecția cu EBV la copii este metoda PCR. Această metodă implică detectarea ADN-ului viral în mostre de salivă, ser de sânge și urină ale unui copil. Copilul trebuie testat pentru virusul Epstein Barr pe stomacul gol și nu trebuie să mănânce alimente grase cu o zi înainte.
Infecția cu mononucleoză infecțioasă, dacă sunt respectate regulile studiului, este detectată în acest caz cu o fiabilitate ridicată.
Metoda de testare PCR este utilizată ca metodă principală de diagnosticare a infecției cu virusuri mononucleoze infecțioase la nou-născuți, precum și la copiii sub 2 ani. Datorită imaturității sistemului imunitar al copilului, testarea prezenței ADN-ului viral în organism este o modalitate mai fiabilă de a diagnostica boala și de a determina diferitele etape ale infecției.
Un pericol deosebit sunt formele șterse de infecție cu EBV, care uneori apar la copii fără manifestarea unor simptome pronunțate care rămân nerecunoscute. PCR în acest caz completează eficient metodele de cercetare serologică.
Una dintre cele mai frecvente infecții ascunse este virusul Epstein-Barr.
Virusul Epstein-Barr, descoperit în 1964 de oamenii de știință Michael Epstein și Yvonne Barr, aparține celui de-al patrulea tip de herpesvirus. Cu toate acestea, oamenii nu sunt suficient de conștienți de infecția cronică cauzată de virusul Epstein-Barr (EBV) și de formele sale.
Virusul Epstein-Barr aparține familiei herpesvirusurilor. Nume scurt: EBV, HHV-4, EBV, HHV-4.
Virusul Epstein-Barr (Virusul Herpesului Uman tip 4). A fost descris pentru prima dată în 1964 și numit după autorii săi, virologul Michael Anthony Epstein, precum și studenta sa absolventă Yvonne Barr din Marea Britanie. Acest virus este unul dintre cele mai frecvente viruși care se găsesc la oameni. El este creditat cu participarea la formarea celulelor tumorale în corpul uman. Multe persoane infectate cu virus se confruntă cu boala cu puține simptome. În stadiul inițial, virusul nu reprezintă o amenințare specială, deoarece nu afectează organele importante sau sistemul circulator. Dar atunci când apar complicații, virusul este capabil să distrugă celulele creierului.
Anticorpii (Ab) împotriva virusului Epstein-Barr (EBV) se găsesc la 60% dintre copii în primii doi ani de viață și la 80-100% dintre adulți.
Virusul Epstein-Barr se transmite în principal prin salivă, uneori prin transfuzii de sânge și este foarte contagios (ușor de prins).
Boli cauzate de virus
Virusul Epstein-Barr provoacă boli precum mononucleoza infecțioasă și limfomul Burkitt. Limfomul Burkitt este diagnosticat printre rezidenții țărilor africane (Uganda, Nigeria, Guineea Bissau). Boala afectează în principal copiii de 4-8 ani. Tumora, a cărei apariție este provocată de virus, afectează ganglionii limfatici, rinichii și glandele suprarenale, ovarele, maxilarele inferioare sau superioare.
În ceea ce privește mononucleoza infecțioasă, numită și „boala sărutului”, de obicei infectează copiii și tinerii. În țările în curs de dezvoltare, până la jumătate din populația copiilor cu vârsta sub 5 ani sunt purtători ai virusului dobândit de la mamele lor. În țările dezvoltate, această rată de infecție este tipică pentru persoanele cu vârsta peste 18 ani.
Vă puteți infecta cu virusul prin salivă, obiecte, în timpul unei transfuzii de sânge sau prin strângerea mâinii. După o perioadă de incubație, care poate dura până la 1 sau 2 luni, virusul se înmulțește rapid. Mai mult, acest lucru se întâmplă în ganglionii limfatici și celulele membranelor faringelui și nasului.
Simptomele virusului includ frisoane și o creștere bruscă a temperaturii (până la 38 de grade și peste). Cei infectați raportează dureri de cap severe, dureri la înghițire și transpirație crescută. În general, dezvoltarea virusului este deghizată ca simptome de infecții respiratorii acute, febră, dureri în gât sau faringită. Informații mai complete despre această problemă pot fi găsite în articolul „Virusul Epstein-Barr. Simptome și tratament.”
Odată ce intră în sânge după reproducere, virusul se răspândește în tot organismul. Particulele sale încep să se răspândească în mediu împreună cu secrețiile corpul uman(salivă, mucus cervical).
În timpul examinării unei persoane bolnave, ganglionii limfatici măriți sunt găsiți în diferite părți ale corpului. Mai mult, sunt nedureroase și din acest motiv nu provoacă un disconfort semnificativ unei persoane. Cursul bolii se termină cu o modificare a formulei de sânge din cauza scăderii numărului și proprietăților celulelor albe din sânge. Organismul, de regulă, luptă singur cu virusul, iar îmbunătățirea are loc după câteva săptămâni (până la 2 luni).
Tipuri de virus Epstein-Barr Acest virus (abreviat EBV, EBV) infectează limfocitele B din sângele uman. În funcție de boala care provoacă reproducerea acesteia,
- Există mai multe antigene ale virusului: EBV-VCA (antigen capside). Capside virale antigene IgG iar IgM provoacă producerea de anticorpi împotriva lor numai în stadiul acut. Nivelurile de IgM scad după 1-3 luni, dar nivel scăzut
- IgG poate persista pe tot parcursul vieții. Niveluri ridicate de antigen capsid viral IgG sunt diagnosticate în cazurile de limfom Burkitt, carcinom nazofaringian și imunosupresie. Titrurile pozitive ale ambelor clase de antigen indică o infecție acută.
- EBV-EA (antigen timpuriu). Anticorpii împotriva acestui antigen încep să fie produși în stadiul acut, cu toate acestea, creșterea numărului lor are loc mult mai lent. Nivelurile lor scad la două luni după infectarea cu virusul. Dispariția lor completă după un an este, de asemenea, posibilă.
EBV-EBNA. Acesta este antigenul nuclear al virusului. Anticorpii împotriva acestuia sunt produși la numai o lună după infectarea cu virusul. Ele se caracterizează prin niveluri ridicate și pot rămâne în sânge pe tot parcursul vieții unei persoane ca indicatori ai imunității.
Multe manifestări și simptome ale virusului Epstein-Barr sunt observate pe o perioadă lungă de timp. O persoană se simte slăbită, uneori somnul îi este perturbat, temperatura corpului îi crește și ganglionii limfatici devin măriți. Dacă aceste simptome reapar, putem vorbi cu încredere despre cronicizarea bolii. Virusul duce la sindromul de oboseală cronică - o persoană se simte în mod constant slăbită și chiar și un somn de zece ore nu restabilește puterea. De asemenea, vacanța nu oferă unei persoane un sentiment de relaxare și un val de energie.
Pentru a determina cu exactitate prezența acestui virus în organism, nu este suficient să cunoașteți principalele simptome de care aveți nevoie metode moderne diagnostice - de exemplu, testul imunosorbent legat de enzime. Dacă 90% din populația adultă este deja purtătoare a virusului Epstein-Barr, atunci numărul adolescenților este mai mic - aproximativ 50%.
Pentru a detecta virusul, se face un test de sânge sau salivă. La confirmarea prezenței sale în organism, este destul de dificil pentru medici să determine în ce stadiu se află boala. A fost puțin studiat, așa că toată munca medicilor vizează în principal eliminarea simptomelor sale. Medicamentele pentru tratarea bolii în stadiul cronic nu au fost încă dezvoltate. Se folosesc imunomodulatoare, se prescrie o dietă nutritivă specială, kinetoterapie și activitate fizică optimă.
Există semne de durere în gât și uneori apare o erupție cutanată. În cele mai multe cazuri, totul se termină cu bine. Evoluția severă apare numai cu infecția cu HIV și alte imunodeficiențe severe. Virusul Epstein-Barr are receptori care îi permit să pătrundă într-unul dintre tipurile de celule protectoare umane - limfocitele B. Acest lucru îi permite să rămână în organism pentru o perioadă lungă de timp și să intre în aproape toate organele și țesuturile. Dar o astfel de apropiere are adesea un efect negativ asupra sănătății, iar celulele imune încep să atace țesuturile unei persoane. Bolile care apar în acest caz se numesc autoimune.
Exemple dintre acestea includ artrita reumatoidă, lupusul eritematos sistemic și altele. În plus, celulele B își pot pierde structura normală, își pot dobândi proprietățile țesuturilor tumorale și pot duce la procese maligne - limfoame, limfosarcom, limfogranulomatoză. Virusul Epstein-Barr este, de asemenea, considerat responsabil pentru manifestările sindromului de oboseală cronică. Unii medici dau vina pentru apariția sclerozei multiple, leziuni hepatice fără cauza.
Tratament pentru infecția cu virusul Epstein-Barr
Nu există un tratament specific pentru virusul Epstein-Barr. Pacientului i se odihnește, i se oferă mult de băut și, dacă este necesar, se prescriu medicamente antipiretice. În unele cazuri, este necesar să se prescrie hormoni, medicamente antivirale și interferon. Mononucleoza infecțioasă necesită tratamentul pacientului într-un spital. Pentru a suprima virusul, este prescrisă o cură de antibiotice, antihistaminice și imunomodulatoare. În esență, tratamentul are ca scop eliminarea simptomelor bolii. Dacă virusul Epstein-Barr provoacă dezvoltarea unei tumori, pacientului i se prescrie un curs de medicamente antitumorale.
Pentru a diagnostica boala, trebuie să fii examinat de un specialist în boli infecțioase și de un medic pediatru (pentru copii). De asemenea, va trebui să faceți un test de sânge, care va arăta prezența anticorpilor. În plus, poate fi prescris un examen imunologic.
Tratamentul infecției cauzate de virusul Epstein-Barr este ghidat de mai multe principii:
- utilizarea unui complex de medicamente care vizează eliminarea simptomelor și tratarea bolilor dezvoltate;
- metode de tratament non-medicament;
- tratament pe termen lung și continuu de natură continuă într-un spital, clinică și centru de reabilitare;
- elaborarea unui program individual de tratament care ia în considerare vârsta pacientului, stadiul infecției, indicatori imunologici, clinici și de altă natură.
Tratamentul nu este întotdeauna necesar, deoarece la copii infecția apare adesea latent, simptomele sunt estompate și boala nu poate fi recunoscută clar. În acest caz, ei se limitează la observarea de către medicul curant și folosesc medicamente care ameliorează inflamația și ajută la eliminarea toxinelor din organism. Ar fi potrivit să se folosească medicina tradițională pentru a elimina simptomele bolii.
Infecțiile cronice necesită un tratament serios într-un spital, precum și dacă există complicații în alte organe.
La diferite antigene ale virusului Epstein-Barr, ceea ce face posibilă identificarea tipului de proces infecțios (transport cronic, acut, asimptomatic). Metoda PCR vă permite să detectați ADN-ul virusului. Prin urmare, metoda PCR este folosită pentru a înțelege cu exactitate dacă există sau nu un virus în corpul uman. Analiza PCR este utilă pentru identificarea virusului la copiii al căror sistem imunitar este imatur și, prin urmare, nu au anticorpi în sânge. În plus, analiza PCR vă permite să determinați cu exactitate prezența virusului Epstein-Barr în organism dacă rezultatele metodei ELISA sunt discutabile.
Deci, să ne uităm la cum să descifrăm analizele Virusul Epstein-Barrși ce înseamnă ele diverse opțiuni rezultate.
Explicația analizei PCR
Rezultatul acestei analize este doi opțiuni posibile– pozitive și negative. Un rezultat PCR pozitiv înseamnă că persoana are virusul Epstein-Barr în organism. Cu toate acestea, nu trebuie să vă fie teamă de acest rezultat, deoarece nu înseamnă neapărat prezența unei infecții acute sau cronice cauzate de virus. Cert este că, odată ce intră în organism, virusul Epstein-Barr, ca și alți virusuri herpes, rămâne în el pentru tot restul vieții și este imposibil de îndepărtat. Cu toate acestea, în majoritatea cazurilor, o persoană este pur și simplu un purtător asimptomatic, iar virusul nu provoacă nicio boală. De aceea test pozitiv PCR înseamnă doar că o persoană a întâlnit acest virus și a intrat în corpul său.Un rezultat negativ al testului PCR înseamnă că virusul Epstein-Barr nu a intrat niciodată în corpul uman.
Interpretarea testelor ELISA
Folosind metoda ELISA, prezența a următoarele tipuri antigeni virali:- IgG la antigenul capsidei (VCA);
- IgM la antigenul capsidei (VCA);
- IgG la antigenele timpurii (EA);
- IgG la antigenele nucleare (EBNA).
Anticorpi IgG la antigenul capsidei VCA (anti-IgG-VCA):
Decodificarea analizei. Un rezultat negativ poate indica faptul că persoana nu a fost niciodată infectată cu virusul Epstein-Barr. Cu toate acestea, un rezultat negativ poate indica faptul că infecția cu virus a avut loc cu mai puțin de 2 săptămâni în urmă. Un rezultat pozitiv înseamnă că o persoană este infectată cu virusul Epstein-Barr, dar nu ne permite să evaluăm stadiul infecției (faza acută, procesul de recuperare sau infecția trecută). Se va obține un rezultat pozitiv al testului în cazul purtării simplu asimptomatic, și în caz de infecție cronică, și în caz de recuperare, și în cazul reactivării virusului.Anticorpi IgM la antigenul capsidei VCA (anti-IgM-VCA):
- Mai puțin de 0,8 - rezultat negativ;
- Mai mult de 1,1 - rezultat pozitiv;
- 0,9–1,0 este un rezultat discutabil.
Anticorpi IgG la antigenele EA timpurii (anti-IgG-EA):
- Mai puțin de 0,8 - rezultat negativ;
- Mai mult de 1,1 - rezultat pozitiv;
- 0,9–1,0 este un rezultat discutabil.
Anticorpi IgG la antigenul nuclear EBNA (anti-IgG-NA):
- Mai puțin de 0,8 - rezultat negativ;
- Mai mult de 1,1 - rezultat pozitiv;
- 0,9–1,0 este un rezultat discutabil.
Pentru a descifra cu exactitate testul pentru anticorpi împotriva virusului Epstein-Barr, puteți utiliza tabelul de mai jos, în care un rezultat pozitiv este indicat printr-un semn „+”, iar un rezultat negativ printr-un semn „-”:
| Stadiul infecției | anti-IgM-VCA | anti-IgG-VCA | anti-IgG-EA | anti-IgG-NA |
| Absența virusului în organism | - | - | - | - |
| Stadiul incipient al infecției primare | + | - | - | - |
| Stadiul acut al infecției primare | ++ | ++++ | ++ | - |
| Infecția a suferit mai puțin de șase luni în urmă | + | ++++ | ++ | - |
| Infecție anterioară (infecție anterioară) | - | +++ | -/+ | + |
| Infecție cronică | -/+ | ++++ | +++ | -/+ |
| Reactivarea infecției cronice (exacerbare) | -/+ | ++++ | +++ | -/+ |
| Tumori cauzate de VEBI | -/+ | ++++ | +++ | -/+ |